このページのトップ
乳がん骨転移
進行期の乳がん患者の大半で合併する骨転移は、生命予後を悪化させる。骨転移には破骨細胞の活性化が関与していると想定されていることから、破骨細胞の活性化を抑制する薬剤が、骨転移の治療薬として用いられている。しかし、その効果は限定的で、顎骨壊死などの重篤な副作用があることから、骨転移の細胞・分子機構の解明に基づく、新たな治療法の開発が望まれている。
エストロゲンレセプター・プロゲステロンレセプター・Her2陰性のマウス乳がん細胞株4T1株をマウス乳房脂肪組織に接種後の骨髄から得られたがん細胞を、vitroで増殖させる操作を3回繰り返すことで、乳房脂肪組織に接種すると骨に高率に転移する4T1.3株が得られた。
4T1.3株は、親株に比べて、vitroでの増殖能、乳房組織接種後の腫瘍形成能、extravasation能に有意の差異を認めなかった。しかし、骨内に接種した時には、親株に比べて、4T1.3株による腫瘍形成が亢進していた。vitroでの培養条件下では、親株に比べて、4T1.3株はケモカインCCL4の発現が亢進している一方で、CCL4の特異的レセプターであるCCR5は発現していなかった。
4T1,3株を骨内に接種した時には、親株接種時に比べて、破骨細胞・骨芽細胞数には優位な差が認められない一方で、I型コラーゲン陽性細胞の増加が認められた。CCL4発現を抑制した4T1.3株の骨内への接種時、あるいは4T1.3株のCCR5欠損マウスへの接種時には、I型コラーゲン陽性細胞の増加が認められないうえに、腫瘍形成も減弱した。
4T1.3株を骨内に接種した時には、骨内でconnective tissue growth factor (CYGF/CCN2)の発現が亢進ている上に、CCR5陽性でI型コラーゲン陽性細胞が選択的にCTGF/CCN2を発現していた。vitroの培養条件下で、CCL4は線維芽細胞の増殖とCTGF/CCN2発現を誘導する一方で、CTGF/CCN2は低酸素培養条件下での4T1.3株の増殖を亢進させた。
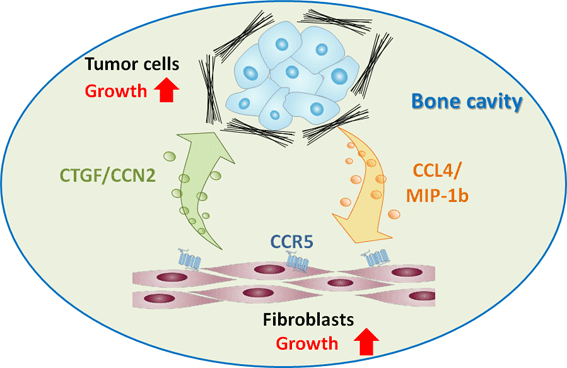
以上の結果から、乳がん細胞が産生するCCL4が、CCR5発現線維芽細胞に作用して、CTGF/CCN2産生を誘導し、これが乳がん細胞の増殖を促進するという、positive
feedback機構の存在が示唆された(下図)(Sasaki et al., 2016)。さらに、線維芽細胞を標的とした新たな骨転移治療戦略の可能性も示唆された。