組織・研究分野
先進がんモデル共同研究センター
Innovative Cancer Model Research Center
腫瘍遺伝学研究分野
Division of Genetics
スタッフ

教授
大島 正伸
Oshima Masanobu

准教授
大島 浩子
Oshima Hiroko

准教授
中山 瑞穂
Nakayama
Mizuho

特任助教
WANG Dong
(ナノ研籍)
目的と研究課題
腫瘍遺伝学研究分野では、胃がん、大腸がん、胆管•膵臓がんなどの消化器がんの発生および悪性化に関して、ゲノム変異と宿主反応の相互作用に着目しながらメカニズム解明を目指して、新規マウスモデルやオルガノイドを樹立し、移植による転移モデルなどを用いて以下の研究プロジェクトを推進しています。
【遺伝的多様性を持つポリクローナル転移機構】
原発巣から遺伝的に多様ながん細胞で構成する細胞集団が遠隔臓器に転移する、「ポリクローナル転移」の概念が提唱されています。悪性度の異なるオルガノイドを用いた移植転移モデルの解析により、転移性クローンが形成する微小環境が、共存する非転移性細胞集団の生存を促進し、ポリクローナル転移巣を形成することを明らかにしました(Kok SY, Oshima H, et al, Nat Commun, 2021)。
【腸管腫瘍悪性化による物性変化Nano解析】
大腸がん発生と悪性化を誘導するドライバー遺伝子を導入したオルガノイド細胞の細胞表面構造を、高速走査型イオン伝導顕微鏡(HS-SICM)を用いて解析した結果、転移能を獲得したがん細胞に特徴的なナノレベルの構造物形成と、細胞膜の硬度に関する物理学的性質の変化を明らかにしました(Wang D, et al, Biomaterials, 2022)
【ネガティブ選択による悪性がん細胞集団進化】
ドライバー変異の蓄積により転移性を獲得した腸管がん由来オルガノイド(AKTP)を用いて、がん細胞組織を構成する個々の細胞の悪性度に関する多様性を、サブクローニングにより解析した結結果、転移能を消失した細胞集団が一定頻度で出現し、ネガティブ選択により集団から排除される新いがん進化機構を明らかにしました(Morita A, Nakayama M, et al, Cancer Sci, 2023)。
図1. 転移性サブクローンによるポリクローナル転移
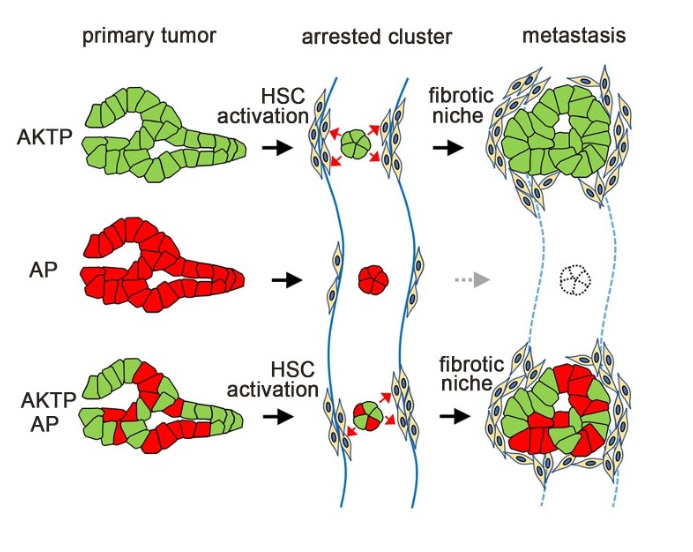
転移性のAKTP細胞と、非転移性AP細胞がクラスターを形成して肝臓に到達すると、AKTP細胞が形成した線維性ニッチが共存するAP細胞の生存と増殖を促進し、ポリクローナル転移巣を形成する。
(Kok SY, Oshima H, et al, Nat Commun, 2021より引用)
図2. 転移性消失サブクローンのネガティブ選択機構
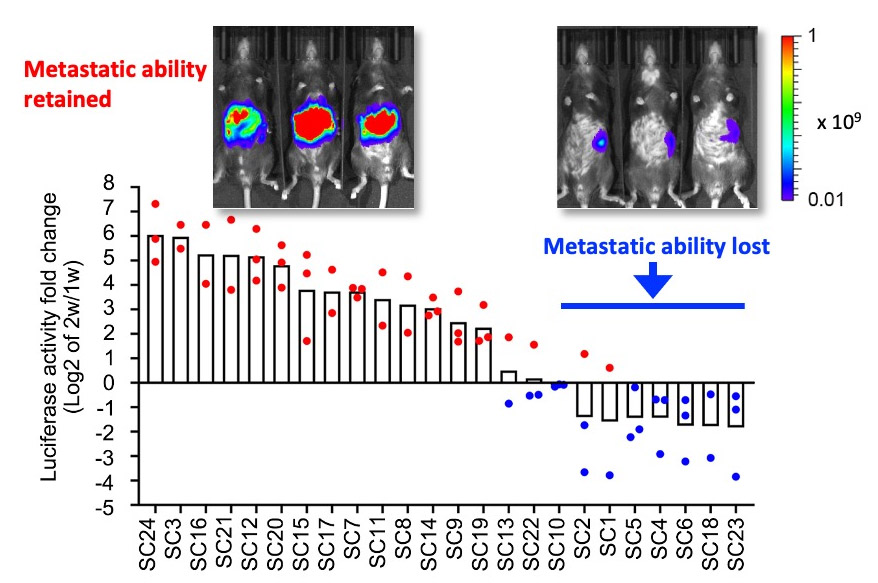
イメージング解析により、転移性のAKTP細胞を構成するサブクローンの約30%で転移性の消失が認められた。これらの細胞は、生体内の腫瘍組織からネガティブ選択機構により排除されている。
(Morita A, Nakayama M, et al, Cancer Sci, 2021より引用)


