ニュースレター
News Letter
News Letter Vol.22
所長よりご挨拶
金沢大学がん進展制御研究所
所長 鈴木 健之
 令和6年1月の能登半島地震発生から1年以上が経過しましたが、9月には豪雨災害も重なり、能登地方の復興・再建は依然として道半ばの状況です。私たち金沢大学がん進展制御研究所も被災地の復興に向け、少しでも貢献できるよう取り組んでまいりたいと思いを新たにしています。幸い、皆様からの温かいご支援のおかげで、当研究所の活動は順調に再開され、従来の研究基盤の復元に加えて、さらなる発展を目指す取り組みを進めることができています。本研究所の研究活動や共同研究拠点活動に対しまして、今後とも変わらぬご支援ご協力を賜りますよう、どうぞよろしくお願い申し上げます。
令和6年1月の能登半島地震発生から1年以上が経過しましたが、9月には豪雨災害も重なり、能登地方の復興・再建は依然として道半ばの状況です。私たち金沢大学がん進展制御研究所も被災地の復興に向け、少しでも貢献できるよう取り組んでまいりたいと思いを新たにしています。幸い、皆様からの温かいご支援のおかげで、当研究所の活動は順調に再開され、従来の研究基盤の復元に加えて、さらなる発展を目指す取り組みを進めることができています。本研究所の研究活動や共同研究拠点活動に対しまして、今後とも変わらぬご支援ご協力を賜りますよう、どうぞよろしくお願い申し上げます。
令和5年度に採択されました文部科学省の共同利用・共同研究システム形成事業「学際領域展開ハブ形成プログラム」は3年目を迎えました。本事業では、「がん」「老化」「炎症」「代謝」に関する研究領域を越えた学際的な連携により、「健康寿命科学」という新たな学術分野を確立し、集合知のプラットフォームを構築することを目指しています。連携機関である東北大学加齢医学研究所、大阪大学微生物病研究所、慶應義塾大学先端生命科学研究所の先生方との密接な協力と知見の共有を通じて、個人の健康・幸福や社会の持続可能性に寄与する研究成果を創出していきたいと考えています。本事業に関連して、昨年11月には、金沢大学にて国際シンポジウムInternational Symposium on Tumor Biology and Interdisciplinary Sciencesを、さらに本年2月には、東北大学で「学際領域展開ハブ形成プログラム 第2回シンポジウム」を開催し、多様な研究分野の研究者が交流を深め、新たな学際的融合研究の可能性について活発に議論する機会を設けることができました。関係者の皆様に厚く感謝申し上げます。
従来からの国際連携としては、10月に復旦大学上海がんセンターとのジョイントシンポジウムを上海で開催しました。最先端のがん研究に関して活発な議論が交わされ、大変有意義な機会となりました。若手研究者の研究室への訪問と懇談では、人材育成のための貴重な意見交換ができ、新しく建設された復旦大学がん研究所附属病院の見学では、中国の驚異的な経済発展の成果を目の当たりにすることとなりました。
また、8月には高校生を対象とするがん研究早期体験プログラム(がん研 EEP2024)を開催しました。令和6年度で3年目になりますが、参加した高校生が、アカデミア・医療・産業界において未来を切り拓く次世代の研究者へと成長することを願っています。
ここ数年、当研究所では分野主任(教授)の定年退任が連続しており、それに代わる若手の教授の着任および昇任が相次いでいます。新しく生まれ変わりつつある当研究所の活動と取り組みを皆様にご理解いただき、引き続きご支援いただきますよう、どうぞよろしくお願いいたします。
令和7年4月
着任のご挨拶
『がんを駆逐する』という一つの目標に、学際的な研究の力を集結し、がん患者さんの希望の力となる
先端がん治療研究分野
教授 谷口 博昭
 令和6年8月に先端がん治療研究分野 教授に着任いたしました、谷口博昭と申します。札幌医科大学医学部を卒業後、同大学第一内科にて消化器がんを中心に臨床・研究に従事し、その後、スペイン国立がん研究センターにてがんエピゲノミクスの研鑽を積みました。帰国後は母校の腫瘍診療部を経て、東京大学医科学研究所にて多くの異分野の先生方のご指導を得て、自身のライフワークとなりました異分野融合研究、抗がん医薬の開発研究に取り組む機会をいただきました。その後、慶應義塾大学医学部に異動し、これらに加えて、がんゲノム医療やトランスレーショナルリサーチ (TR)支援に与する機会をいただきました。
令和6年8月に先端がん治療研究分野 教授に着任いたしました、谷口博昭と申します。札幌医科大学医学部を卒業後、同大学第一内科にて消化器がんを中心に臨床・研究に従事し、その後、スペイン国立がん研究センターにてがんエピゲノミクスの研鑽を積みました。帰国後は母校の腫瘍診療部を経て、東京大学医科学研究所にて多くの異分野の先生方のご指導を得て、自身のライフワークとなりました異分野融合研究、抗がん医薬の開発研究に取り組む機会をいただきました。その後、慶應義塾大学医学部に異動し、これらに加えて、がんゲノム医療やトランスレーショナルリサーチ (TR)支援に与する機会をいただきました。
この度、がんに特化した国内屈指の研究所にて汗を流す機会をいただきましたこと、深く御礼を申し上げます。宝町キャンパスにおいて臨床と深くリンケージできる環境は、自身が取り組むがんのTRおよびリバースTRを展開するようにという啓示と考え、より一層、新規がん治療法の開発によるがん制圧に全集中してまいります。
がんの分子・生物学的基礎研究を基盤として、数理科学、理工学や薬学などの異分野研究者との協働を通じて、革新的な抗がん医薬の開発に取り組んでまいりました。その一例が、特定のがん標的分子を特異的に発現抑制する抗がんsiRNA医薬の開発です。この分野では、配列設計やドラッグデリバリーシステムなど多くの課題がありましたが、共同研究を通じてこれらを克服し、First in Humanの治験に繋げました。
現在、がんを根治するという1つの目標の下に、教室員の先生方と共に、複数の標的分子を同時に抑制可能な革新的な抗がんマルチターゲット型siRNA医薬の開発、前任の矢野聖二教授の研究を継承させていただき、幅広いがん種で課題となっている薬剤耐性機序の解明や、KRAS変異がんに対する新しい治療法の開発を進めております。さらに、CAR-Tなどの先進的な免疫細胞療法、分子間相互作用を基盤とする抗がん薬スクリーニング系の構築など、次世代治療法の開発を推進しています。
私共は病院での腫瘍内科の診療を担っており、腫瘍診療科と緊密に連携させていただくことで、臓器横断的に固形がんに対する患者さんの目線に立った薬物療法を実施しております。この連携を基盤に病院と研究所を繋ぐリバースTRを展開してまいります。
がん患者さんと教室員の幸せを第一に研究に取り組んでまいりますので、ご指導ご鞭撻を賜りますよう、お願い申し上げます。

研究分野のメンバー(筆者前列の右から2番目)
Cancer Evolution(がんの進化)― がんゲノムに遺伝子異常を起こす分子機構を理解し、がんや薬剤耐性を予防する治療に繋げる
ゲノム生物学研究分野
教授 磯崎 英子
 令和6年11月にゲノム生物学研究分野 教授に着任いたしました、磯崎英子と申します。不慣れなことも多い中、所長の鈴木先生をはじめ、各研究分野そして事務の皆様に大変ご親切にしていただき、一歩ずつ前進する日々を過ごしております。
令和6年11月にゲノム生物学研究分野 教授に着任いたしました、磯崎英子と申します。不慣れなことも多い中、所長の鈴木先生をはじめ、各研究分野そして事務の皆様に大変ご親切にしていただき、一歩ずつ前進する日々を過ごしております。
私は、大学卒業後、10年ほど薬剤師として岡山大学病院に勤めておりました。その折に、呼吸器内科の先生と肺がんに関する共同研究をする機会に恵まれ、これがきっかけで研究の道を志すようになりました。研究者としては遅いスタートでありましたが、思い立った今日という日が、今後の己の人生の中で一番若い日であり、10年、20年後に後悔のないよう生きたいと考え、大学院への入学を希望しました。多くの人々と家族の理解に支えられ、博士課程では、岡山大学血液・腫瘍・呼吸器内科学にて肺がんの研究をすることが叶いました。博士課程での研究は大変刺激的で、寝る時間も惜しいと思うくらい研究のことで頭がいっぱいでした。日中は薬剤師として大学病院に勤務し、夜間と土日に研究しておりました。ほとんど寝ていなかったので、ある時、体調を崩し、体が資本であることを学びました。実際に、研究の世界で活躍されている多くの研究者が日々体を鍛え、健康に留意されていることに気づかされます。海外での学会は時差と長距離移動との体力勝負であり、これに疲労してパフォーマンスが低ければ、せっかくの研究成果も台無しになります。北陸の冬は厳しいですが、心と体の健康に留意して研究に励みたいと思います。
さて、体調を崩すほど研究に夢中になってしまった理由ですが、実臨床に限りなく近く、かつ最先端の研究内容であったことが大きかったと思います。研究テーマは、当時、第I/II相試験中であったALK阻害剤(アレクチニブ)の薬剤耐性機構を解明することでした。日本で開発された薬剤であり、世界に先行して着手された研究でした。自身の研究成果をもとに臨床試験を行うことを目標にまっすぐ走り続けた日々でした。今後も、できる限り臨床や人の世に還元性の高い仕事をしていきたいと思っています。学位取得後は、再び臨床の薬剤師として働く予定でしたが、留学する機会に恵まれ、平成29年に渡米しました。肺がんの分子標的薬治療をリードしてきたマサチューセッツ総合病院がんセンター・ハーバードメディカルスクールにて、ポスドクを経てインストラクターとして引き続き、肺がんの分子標的治療薬の耐性機構について研究してきました。ここでの研究から、がん細胞が薬剤耐性を獲得するまでの過程(がんの進化)について着目することで、がんの進展を阻止できるのではないかという考えに至りました。留学前は、海外の計り知れない研究力に圧倒されるばかりでしたが、今は日本でも同等かそれ以上の研究をすることは十分可能であると考えています。留学して最も良かったと思うことは、各国から集まった優秀な研究者と出会えたことです。人脈は宝です。彼らは生涯を通じての友であり、研究仲間になると思います。また、他国に住むことで、自国である日本を見つめ直す機会にもなりました。米国には各国からの人々が集まっています。いずれの国の出身者も、日本の技術や文化に強い興味を持っており、賞賛と期待に溢れていました。私自身、留学を通じて日本により興味を持つようになり、自国であることを誇りに思うようになりました。日本独自の研究を基盤とした自身の成果を世界に発信することで、国内外において研究の輪を広げていきたいと思います。

研究分野のメンバー:右から酒井先生(准教授)、喜田さん(修士学生)、胡蝶さん(蘭)、筆者、東さん(事務補佐)
退任のご挨拶
須田貴司教授は令和7年3月末をもって、当研究所を定年でご退任されました。平成10年(1998年)、金沢大学がん研究所(当研究所の旧名称)に新設された分子標的薬剤開発センターの教授として着任され、8年間にわたり、慢性炎症とがんの病態の分子機構の解明研究において多大な研究成果を残されました。平成18年(2006年)から現在に至るまでは、免疫炎症制御研究分野の教授として、様々なプログラム細胞死の分子機構を中心にがんの本態解明を目指す基礎研究に取り組むとともに、若手研究者育成のための本学の教育活動にも貢献されました。
永年にわたり多くのご功績を残されましたことに敬意を表しますとともに、本研究所の発展に貢献されましたことに心より感謝申し上げます。
細胞死と炎症とがんの三角関係の解明を目指した27年間
免疫炎症制御研究分野
教授 須田 貴司
 私は平成10年(1998年)4月に当時のがん研究所に着任し、以来27年間にわたり当研究所の教授を務めさせていただきました。先ずはこの間、当研究所の職員の方々を筆頭に、多くの方々からご支援いただきましたことに心より感謝申し上げます。
私は平成10年(1998年)4月に当時のがん研究所に着任し、以来27年間にわたり当研究所の教授を務めさせていただきました。先ずはこの間、当研究所の職員の方々を筆頭に、多くの方々からご支援いただきましたことに心より感謝申し上げます。
私は、前任地でFasリガンドを同定し、この蛋白因子により誘導される細胞死(アポトーシス)の研究をしていたことから、当面はFasリガンドの研究を続けることにしました。当時、アポトーシスは炎症を誘導しないと言われていましたが、私はFasリガンドが炎症誘導作用を持つと考えていました。当時としては“非常識”な発想だったと思いますが、研究を進めていくとFasリガンドはアポトーシスを誘導するだけでなく、NF-κBの活性化を誘導し、好中球や樹状細胞にIL-1βやIL-23などの炎症性サイトカインの産生を誘導する作用を持つことが明らかになりました。また、慢性肝炎から肝がんを発症する動物モデルを用いて抗Fasリガンド中和抗体の治療効果を検討したところ、肝炎を抑制するとともに肝がんの発症も予防できることが明らかになりました。これは、慢性炎症の抑制で発がんを予防できることを実証したという点でも重要な研究成果だったと自負しております。
次に、私はASCと呼ばれる新規蛋白に注目しました。ASCは抗がん剤でアポトーシスを起こしたがん細胞内で巨大な凝集塊を形成する蛋白として発見されたものです。このASCを様々なヒトがん細胞株で活性化すると、アポトーシスで死ぬものとネクローシスで死ぬものがあることが分かりました。これらの細胞の遺伝子発現プロファイルを比較したところ、ネクローシスで死ぬ細胞株のみがカスパーゼ1を発現していました。さらにネクローシスを起こす細胞株のカスパーゼ1をノックダウンすると、細胞死の様式がアポトーシスに変換されました。マクロファージではカスパーゼ1の活性化によりネクローシス様のプログラム細胞死=パイロトーシスが誘導されますが、我々の研究から、がん細胞でもカスパーゼ1を活性化すればパイロトーシスを誘導できることが明らかになりました。
我々はFasリガンドの炎症誘導作用を明らかにしましたが、一般的にはアポトーシスはネクローシスに比べ炎症を誘導せず、免疫抑制的に働くと言われています。多くの抗がん剤は細胞にアポトーシスを誘導しますが、もっぱらがん細胞の増殖阻害を狙った抗がん剤は免疫を抑制しますので、抗腫瘍免疫の誘導には不利に働くと考えられます。一方、パイロトーシスは炎症誘導性プログラム細胞死と言われており、抗腫瘍免疫の誘導には有利に働く可能性が高いと思います。もし、がん細胞に選択的にパイロトーシスを誘導する方法が開発されれば、がん細胞を直接叩くだけでなく、同時に抗腫瘍免疫を活性化する新しい治療法になるかもしれないと期待しています。
紙面の都合で当研究所での研究成果から2つだけご紹介しましたが、お陰様で実り多い研究生活を送らせていただきました。改めてこれまでの皆様のご厚情に深謝するとともに、今後の皆様の益々のご活躍をお祈りしつつ、筆をおきます。
略歴
1982年 埼玉大学理学部生化学科卒業
1984年 大阪大学大学院医学系研究科修士課程修了(医科学修士)
1988年 大阪大学大学院医学系研究科博士過程修了(医学博士)
1988年 米国DNAX研究所免疫学部門 ポストドクトラルフェロー
1992年 大阪バイオサイエンス研究所分子生物学部門 研究員
1995年 同上 副部長
1998年 金沢大学がん研究所分子標的薬剤開発センター 教授
2006年 金沢大学がん研究所*免疫炎症制御研究分野 教授
*2011年に金沢大学がん進展制御研究所に改名

ラボメンバーとのバーベキュー(筆者左から2番目後ろ)

教授室にてラボメンバーと(筆者前列中央)
がん進展制御研究所 若手研究者の紹介
真似をして楽をしたものは、その後に苦しむことになる
がん・老化生物学研究分野
特任助教 隈本 宗一郎
 城村 由和教授が主宰する、がん・老化生物学分野に令和6年4月より特任助教として着任しました隈本 宗一郎と申します。城村研究室は令和4年4月に立ち上がったばかりの研究室ですが、馬場 智久准教授、中野 泰博助教、定免 由枝技能補佐員および6名の学生が所属しており、活気のあるラボに恵まれたと実感しております。
城村 由和教授が主宰する、がん・老化生物学分野に令和6年4月より特任助教として着任しました隈本 宗一郎と申します。城村研究室は令和4年4月に立ち上がったばかりの研究室ですが、馬場 智久准教授、中野 泰博助教、定免 由枝技能補佐員および6名の学生が所属しており、活気のあるラボに恵まれたと実感しております。
私の生まれは福岡県久留米市ですが、祖父母は佐賀県の生まれで、幼少の一時期は佐賀県で暮らしていました。そのため金沢とはまったく無縁だと思っていました。しかし、佐賀には秀吉の朝鮮出兵のための戦略拠点となった名護屋城があり、加賀百万石の祖である前田 利家が城の表を守る重要な陣城を築いており、少なからず縁を感じています。
私はいわゆる高専で物質工学を専攻していました。しかし、もともと生物が好きなこともあり、大学へ編入学して生物の勉強を始めました。大学では、マウス生殖細胞および発生期におけるエピゲノム、特にゲノムインプリンティングに関する研究に取り組みました。大学院博士課程ではカエル 卵抽出液を用いた岡崎フラグメント合成・連結の分子メカニズムの研究に従事していました。令和3年に学位取得後は次世代シーケンサーを用いた大規模解析の研究支援業務に携わり、その後、細胞分裂と中心体研究、そして令和6年から細胞老化に関する研究を始めました。細胞老化は、個体老化や加齢性疾患の発症・悪化に関与する一方、発がん防御機構としても知られています。城村研究室では、老化細胞の不可逆性やその若返り機構の解明を目指しています。
タイトルは、私の名前の由来になった本田 宗一郎の言葉です。上述のように様々な研究分野に手を出した経験をポジティブにとらえ、オリジナルな研究を展開できるよう邁進していく所存です。
せっかく金沢に来たのでスノーボードを再開しようと思っており、お勧めのスキー場があればぜひ教えてください。また、ウイスキーやギター、ベースが趣味の方もぜひお声がけくださると嬉しいです。

注目の研究
老化細胞除去は膀胱がん治療の新たな戦略
がん・老化生物学研究分野
教授 城村 由和
 私は、平成5年(2003年)3月に名古屋市立大学薬学部を卒業後、同大学院に進学し、指導教員である今川正良先生のもとで、生活習慣病の一因である肥満に密接に関与する脂肪細胞の分化について研究を行い、平成20年(2008年) 3月に学位を取得しました。その後、アメリカ国立衛生研究所(NIH)で約2年半、細胞周期に関する基礎研究に従事し、平成23年(2011年)5月に名古屋市立大学大学院医学研究科の中西真先生が主催する細胞生化学講座の助教に就任しました。この時、自分の研究人生の中心となるテーマを模索した結果、大学院生時代から興味を持っていた老化とそれに関連する疾患の研究に取り組むことを決意し、現在の主要テーマである「細胞老化」の研究を開始しました。
私は、平成5年(2003年)3月に名古屋市立大学薬学部を卒業後、同大学院に進学し、指導教員である今川正良先生のもとで、生活習慣病の一因である肥満に密接に関与する脂肪細胞の分化について研究を行い、平成20年(2008年) 3月に学位を取得しました。その後、アメリカ国立衛生研究所(NIH)で約2年半、細胞周期に関する基礎研究に従事し、平成23年(2011年)5月に名古屋市立大学大学院医学研究科の中西真先生が主催する細胞生化学講座の助教に就任しました。この時、自分の研究人生の中心となるテーマを模索した結果、大学院生時代から興味を持っていた老化とそれに関連する疾患の研究に取り組むことを決意し、現在の主要テーマである「細胞老化」の研究を開始しました。
老化はがんの主なリスク要因であり、60歳を過ぎると多くのがんの発症率が急増します。がんは加齢に関連する病気とされていますが、老化とがんの関係はまだ十分に解明されていません。これまでの長年の研究により、原がん遺伝子や腫瘍抑制遺伝子の突然変異が蓄積し、それががんの進行を引き起こすことが明らかになっており、この突然変異の蓄積が、年齢とともにがんの発生率が高まる理由の一つと考えられています1)。実際、健康な組織でも、加齢とともに体細胞の突然変異が増加します。しかし、「ペトの逆説」により、細胞数や寿命が長い動物が短命な動物よりも必ずしもがんの発生率が高いわけではないことも示されています2)。
がんは、免疫細胞や線維芽細胞などの非がん細胞(間質細胞)とがん細胞が相互に作用しあう複雑な環境によって進行し、近年の研究により、間質細胞およびそれらによって分泌される分子が、がんの進行に重要な役割を果たしていることが明らかになっています3)。これらの知見から、加齢による組織微小環境の変化ががんを促進し、間質細胞がその進行に関与する可能性が考えられますが、その実態については不明な点が多くあります。
細胞老化は、DNA損傷を含めた様々な内因性・外因性ストレスによって引き起こされ、それによって生じた老化細胞は不可逆的に細胞増殖を停止するとともに、炎症を引き起こすサイトカインやケモカイン等を分泌します4)。最近の研究では、老化した間質細胞ががんの成長や浸潤、転移を促進する可能性が示唆されていますが、これらの細胞がどのようにがんの悪性化に関与しているのか、その全貌はまだ解明されていません。そして今回、私たちは加齢によってすでに老化した膀胱内の線維芽細胞が、CXCL12とよばれるケモカインを分泌することでがんが発生しやすい環境を作り出していることを見出しました5)。
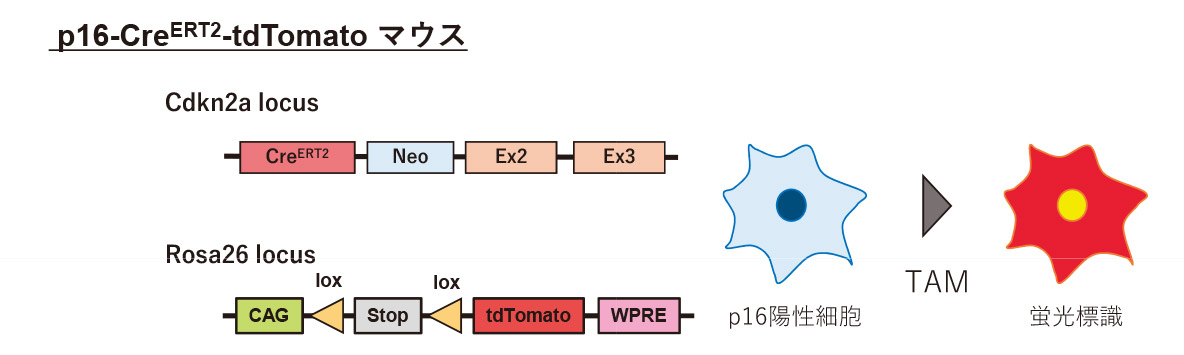
【図1】一細胞レベルで老化細胞を可視化できるマウスモデル
p16-CreERT2-tdTomatoマウスでは、p16陽性細胞内で発現したCreERT2がタモキシフェン(TAM)投与により核内に移行される。その結果、Rosa26にあるlox配列に挟まれたSTOP配列はCreERT2による組み換えで除かれ、tdTomatoが発現し、p16陽性細胞は赤色蛍光でラベルされる。
本研究では、まずはじめに、私たちが独自に開発した老化細胞マーカーp16を発現する細胞(
p16陽性細胞)を一細胞レベルで可視化できるp16-CreERT2-tdTomatoマウスモデルを用いて【図1】、p16陽性細胞が加齢とともに膀胱内、その中でも特に膀胱の粘膜固有層や筋層に存在し蓄積することを明らかにしました。膀胱内に蓄積するp16陽性細胞の細胞種の同定やその特性を明らかにするために、単一細胞RNAシーケンシングを行った結果、p16陽性線維芽細胞ではp16陰性線維芽細胞に比べて、がん細胞の増殖、浸潤、転移、血管新生など、がんの進行を支えるシグナル伝達を活性化するCXCL12の発現が高いことが明らかになりました。
次に、p16陽性細胞を遺伝学的・薬理学的アプローチにより体内から除去する『セノリシス』やCXCL12のシグナル経路の薬理学的な阻害によって、膀胱がんの成長が顕著に抑制されることを動物モデルを用いた実験で証明することができました【図2】。
さらに、私たちは、SMOC2、GUCY1A1(GUCY1A3)、CXCL12、CRISPLD2、GAS1、およびLUMの高い発現レベルを、ヒトおよびマウスにおけるp16陽性線維芽細胞の遺伝子シグネチャーとして特定しました。これらの遺伝子シグネチャーは加齢と相関しており、進行性および非進行性の膀胱がん患者の予後が悪いことと関連していることがわかりました【図3】。
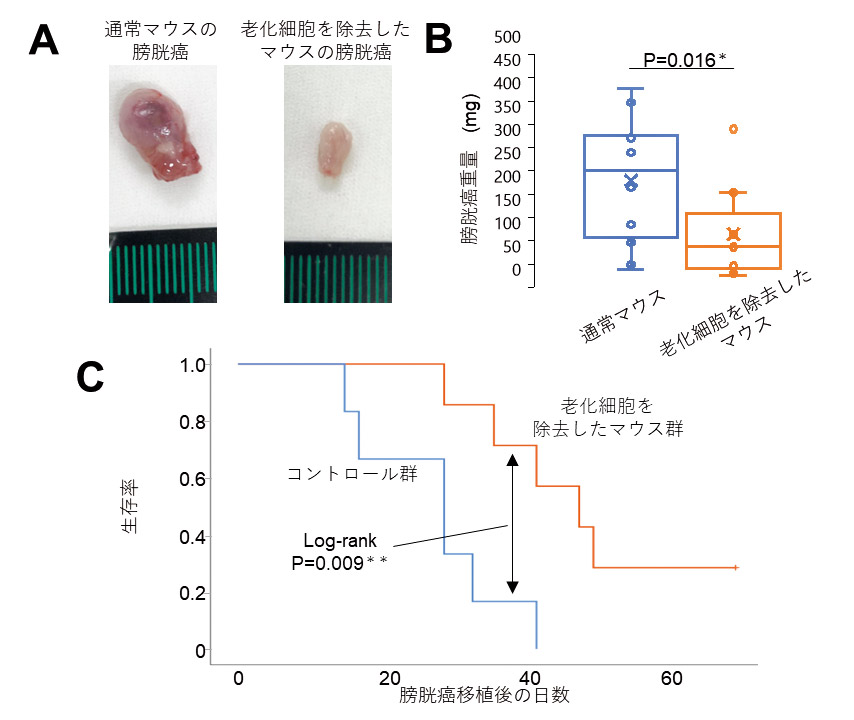
【図2】p16陽性老化細胞の除去は膀胱がんの進行を抑制する
膀胱がん細胞を移植後にp16陽性老化細胞を除去すると、膀胱がんの重量は減少する(A、B)。また移植後の生存率も改善する(C)(Meguro et al., Nature Aging(2024)より改変)。
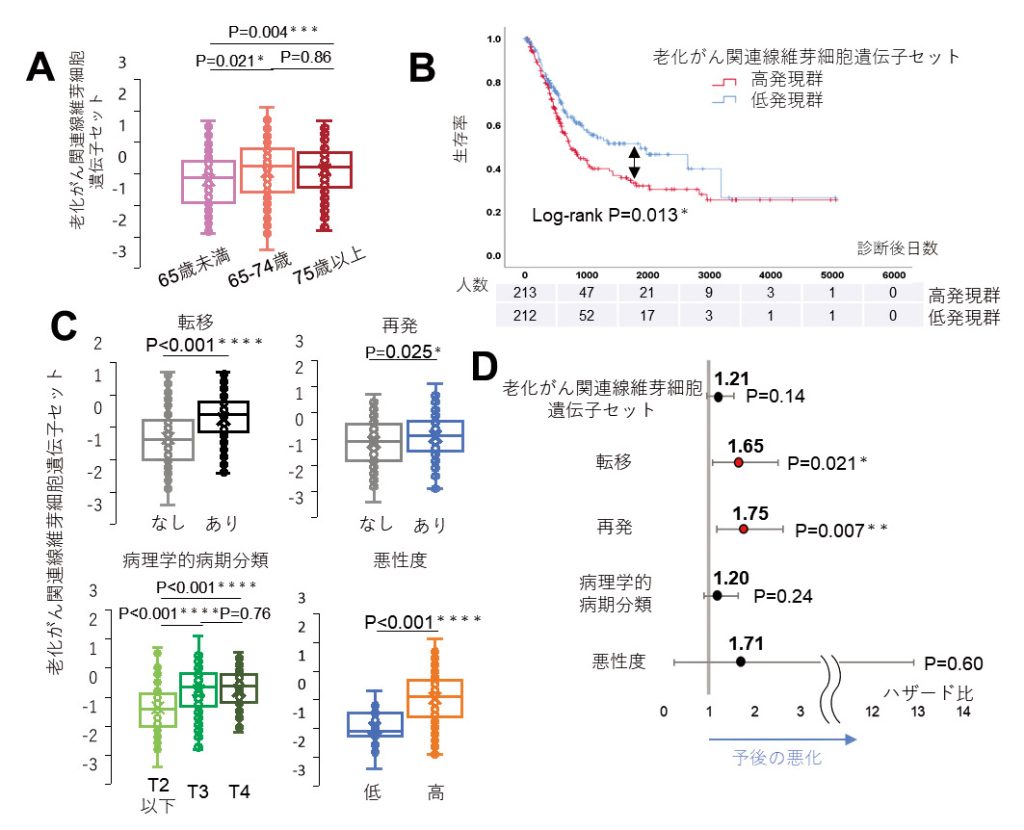
【図3】老化がん関連線維芽細胞遺伝子セットはヒト膀胱がん患者の年齢・予後に関連する
マウスの実験結果より作成した老化がん線維芽細胞遺伝子セットは、ヒト膀胱がん患者の年齢 (A)や予後 (B-C)と相関する。また、ハザード比は病理学的病期分類と同等である(D)(Meguro et al., Nature Aging(2024)より改変)。
これらの研究は、加齢による細胞老化とがん進行の密接な関係を明らかにし、老化関連線維芽細胞を標的とすることで、膀胱がんの新たな治療法の開発に貢献する可能性を示唆しています。
研究を進める中で、『なぜ膀胱がんを研究対象に選んだのか?』と聞かれることがあります。素晴らしい洞察に基づき選択していれば格好もつくのかもしれませんが、単純に私と一緒に研究を進めてくれた本研究の筆頭著者である目黒了さんが福島県立医科大学の泌尿器科の医師であったからです。しかし、研究を行う上で最も大切なのは研究者自身の情熱とモチベーションだと考えています。今後も、研究室員の研究への思いを一番大事にしながら、がんをはじめとする重大な病気に苦しむ人が減り、健康な生活を長く送れる社会を目指して研究に邁進していきます。
参考文献
1) Takeshima H et al., NPJ Precis Oncol (2019)
2) Peto R et al., Br J Cancer (1975)
3) Quail DF et al., Nat Med (2013)
4) Di Micco et al., Nat Rev Mol Cell Biol (2021)
5) Meguro S et al., Nat Aging (2024)

研究分野のメンバー




